|
α-酮戊二酸对公猪精液保存效果的影响
聂晶坤 1,杨希妍 1,何 健 1,马 姝 1,周 健 4,李秋燕 5,朱晓萍 1 *,赵云翔 2,3 *
(1.佛山科学技术学院生命科学与工程学院,广东 佛山 528231;2.广西大学动物科学技术学院,广西 南宁 530004;3.广西扬翔股份有限公司,广西 贵港 537100;4.河南秀博科技有限公司,河南 禹州 461600;5.广西贵港市港南区动物疫病预防控制中心,广西 贵港 537100)
猪的人工授精技术是促进现代养猪业发展的重要技术手段之一,而精液的保存是猪人工授精技术中的关键环节。猪精子细胞膜中含有大量多不饱和脂肪酸,抗氧化能力较弱,对氧化应激更为敏感。活性氧通过精子膜上磷脂的氧化反应改变膜的功能结构,从而破坏精子的功能。活性氧可抑制酶类活性或使酶失活,当活性氧不能被及时清除时,氧化损伤加深,并随着时间延长,会发生脂质过氧化反应,形成丙二醛,损害精子细胞功能。冷冻保存是家畜精液长期保存的最有效方法,在冷冻保护剂中加入抗氧化化合物可以对抗或防止氧化应激。近十年来,维生素E、谷胱甘肽、牛磺酸等抗氧化剂对猪冷冻精子质量和受精能力等方面的研究给予了极大的关注。
α-酮戊二酸(AKG)是三羧酸循环的中间代谢产物,连接细胞内碳-氮代谢的关键节点,与氨基酸、维生素和有机酸的合成及能量代谢相关,具有广泛的应用前景。黄芳等研究表明:添加15 mmol/L AKG可以显著提高猪精子的获能状态,并显著提高获能过程中的糖代谢及抗氧化能力。目前AKG作为外源性抗氧化剂用于猪精液常温保存或冷冻保存的报道很少。本试验通过在猪精保存液中添加不同浓度的AKG,评估其对猪精液在常温保存或冷冻保存下的效果,筛选出AKG作为精液保存抗氧化剂的最适添加量及可行性,以期为猪精液常温保存、冷冻保存稀释液配方的研发提供科学依据。
1
材料
1.1 试验动物
选用27头体况良好、性欲旺盛且繁殖性能好的公猪,由河南秀博公猪站提供。假阴道法采集精液,7头、20头公猪精液进行常温保存和冷冻保存。
1.2 主要试剂
冷却保护稀释液 Androhep? CryoGaurd?粉剂、乳化剂Equex-Paste均购自米尼图;AKG粉末购自上海阿拉丁生化科技股份有限公司;甘油购自Sigma公司;新鲜卵黄。
1.3 主要仪器
HH-6数显恒温水浴锅购自常州澳华;KDC-2046低速冷冻离心机购自安徽中科;精子检测分析仪购自IVOS-II,IMV;熏蒸架购自田园奥瑞;EasyCoder2.0色带打印机、TurboFreezerM程序冷冻仪、冷冻精子平衡柜、单头灌装机MPPUno(米尼图)、0.5 mL冻精细管等均购自于米尼图。
2
方法
2.1 溶液配制
2.1.1 梯度浓度AKG常温保存液配制
取1 000 mL UP超纯水在水浴锅加热至37℃,将稀释粉倒入超纯水中搅拌30 min后分装并添加不同浓度AKG。AKG的浓度分别为0.00 mmol/L、0.05 mmol/L、0.15 mmol/L、0.3 mmol/L、0.45 mmol/L和0.6 mmol/L。
2.1.2 梯度浓度AKG冷冻保护液配制
取770 mL up超纯水在水浴锅加热至34℃,缓缓倒入Androstar?CryoPlus基础稀释粉充分搅拌溶解,待溶液pH稳定后加入200 mL卵黄搅拌1 h,取500 mL溶液作为冷冻液Ⅰ。向剩余溶液中加入30 mL甘油和5 g乳化剂 Equex-Paste搅拌1 h,作为冷冻液Ⅱ,根据所需浓度确定添加的AKG量。
2.1.3 解冻液配制
猪精液保存粉与1 000 mL 37℃的up超纯水搅拌混匀,清澈后震动30 min,待溶液pH稳定后冷冻保存。
2.2 精液处理
2.2.1 精液的常温保存
精液1:1稀释后,分别加入含不同浓度α-酮戊二酸的保存液中,放置在17℃冰箱,摇晃混匀2次/d,以免精子沉积。连续检测6 d。
2.2.2 精液的冷冻
参照周健精液冷冻方法进行。
2.2.3 精液的解冻
将0.5 mL冻精细管在50℃水中解冻16 s后迅速拿出,剪开冻精细管将精液挤入含有2 mL解冻液的EP管中,摇匀后用移液枪多次混匀,取出1 mL丢掉,加入3 mL解冻液,混匀后放入34℃的水浴锅中,等待检测。
2.3 精子运动参数指标的测定
采用计算机辅助精子分析系统(CASA)进行检测,如,精子活力(totalmotility,TM)、直线速度(straight-line velocity,VSL)、曲线速度(curvilinear velocity,VCL)、平均路径速度(averagepath velocity,VAP)值、前向精子数、畸形率。取常温保存精子样品或解冻后精子样品2.5 ?L精液样本移液到预热的一次性计数室,并在整个分析期间保持在37℃。
2.4 统计分析
采用SPSS22.0软件进行单因素方差分析,采用Duncan法对各组间平均数进行多重比较,结果用“平均值±标准差”表示。P<0.05表示差异显著。
3
结果与分析
3.1 α-酮戊二酸对猪精液常温保存的影响
3.1.1 α-酮戊二酸对猪精子活力的影响
从表1中可得,0.05 mmol/L组的精子活力在第2、3、5 天分别高于未添加组0.20%、0.79%、0.73%,但差异不显著(P>0.05)。
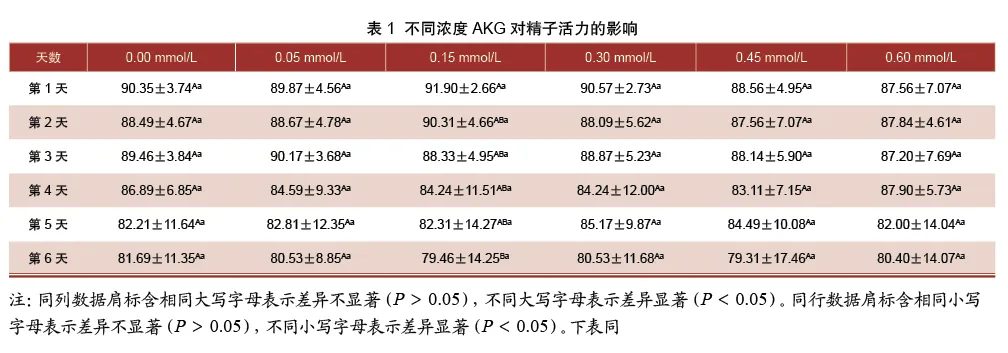
0.15 mmol/L组的精子活力在第1、2、5天分别高于未添加组1.72%、2.06%、0.12%,但差异不显著(P>0.05)。在第5天0.30 mmol/L、0.45 mmol/L组的精子活力分别比未添加组高3.60%、2.77%,但均差异不显著(P>0.05)。除了0.15 mmol/L组的精子活力在第6天显著低于第1天(P<0.05),其余各处理组的精子活力均随着保存数的增加呈下降趋势且差异不显著(P>0.05)。
3.1.2 α-酮戊二酸对猪精子VAP的影响
由表2可得,0.30 mmol/L组的VAP在第5天高于其他处理组,比未添加组高9.63%且差异不显著(P>0.05)。各处理组随着保存天数的增加,精子VAP均呈下降趋势,未添加组在第5、6天的VAP显著低于第1天(P<0.05),分别下降20.93%、22.84%。各处理组第6天的VAP均比第1天显著下降(P<0.05),分别降低了21.61%、25.42%、22.60%、23.12%、19.60%。
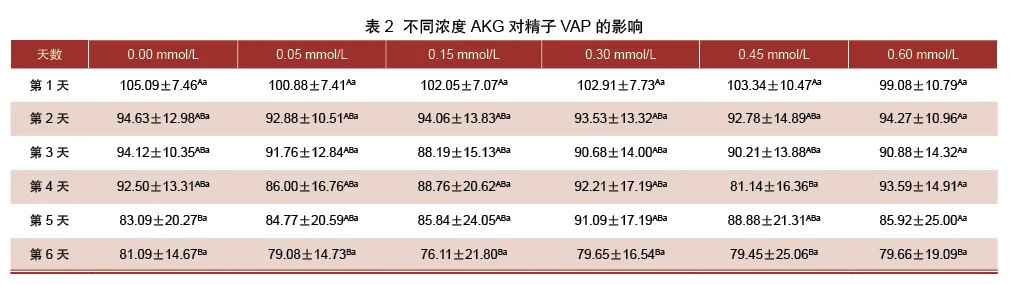
3.1.3 α-酮戊二酸对猪精子VSL的影响
由表3可知,0.05 mmol/L组的VSL在第1、3、5天分别高于未添加组1.62%、0.80%、0.69%、3.28%;0.15 mmol/L组的VSL在第2、4、5天分别高于未添加组3.31%、4.37%、1.27%;0.30 mmol/L的组VSL第2、3、5天均高于其他组,且分别比未添加组高了3.61%、1.68%、6.94%,第4天高于未添加组2.41%,但各处理组与未添加组间差异不显著性(P>0.05)。各处理组随着保存天数增加,VSL呈现下降趋势,与第1天相比,第6天各处理组分别下降了16.30%、20.00%、22.03%、16.20%、17.29%、9.83%,但差异不显著(P>0.05)。
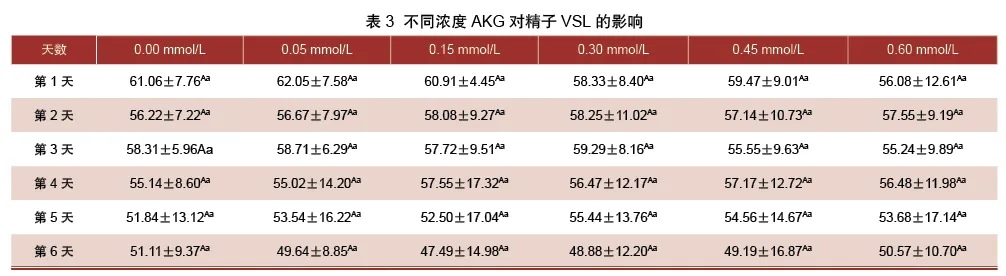
3.1.4 α-酮戊二酸对猪精子VCL的影响
由表4可知,0.45 mmol/L组的VCL与未添加组比,第4天显著降低了18.84%(P<0.05)。0.45 mmol/组的VCL在第5天高于其他组,且比未添加组高9.73%但差异不显著(P>0.05)。各处理组随着保存天数的增加,精子的VCL呈下降趋势,未添加组第5、6天的VCL均显著低于第1天(P<0.05),分别下降了19.23%、17.86%。除0.60 mmol/L组,其他处理组第6天的VCL均比第1天显著下降(P<0.05),分别低了16.86%、21.85%、17.66%、20.93%。
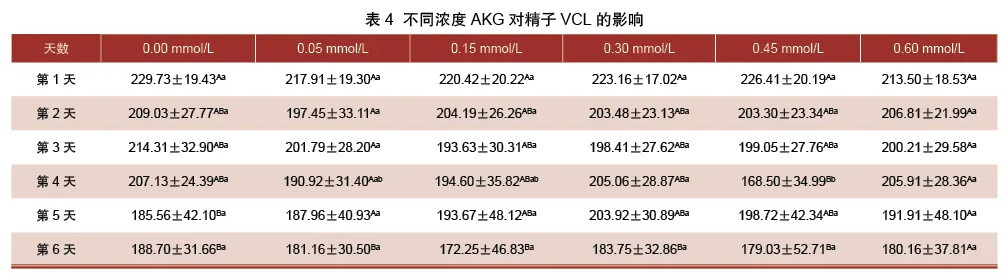
3.1.5 α-酮戊二酸对猪精子前向精子数的影响由表5可知,0.05 mmol/组的前向精子数第1天高于其他组,且比未添加组高了7.97%,但二者间差异不显著(P>0.05)。0.15 mmol/L组前向精子数第2、3天均高于其他组,且分别比未添加组高了4.87%、4.62%,但差异不显著(P>0.05)。0.30 mmol/L组的前向精子数第5天高于其他组,且比未添加组高了1.82%,但差异不显著(P>0.05)。0.45 mmol/L组的前向精子数第4天高于其他组,且比未添加组高了9.99%,但差异不显著(P>0.05)。各处理组随着保存天数增加,前向精子数整体呈现下降趋势。

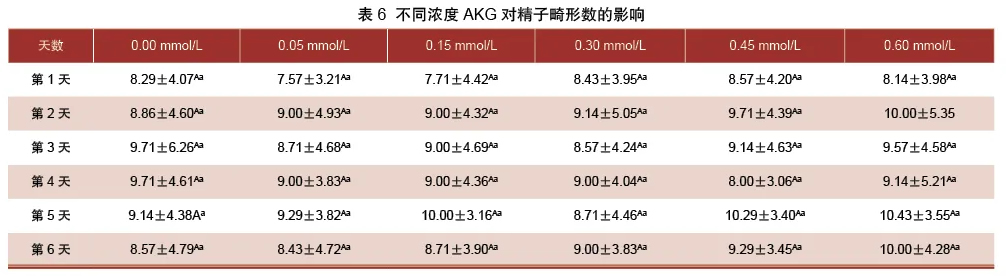
3.1.6 α-酮戊二酸对猪精子畸形率的影响
由表6可知,0.05 mmol/L组的精子畸形率在第1、3、4、6天分别低于未添加组8.69%、10.30%、7.31%、1.63%,但差异不显著(P>0.05)。0.15 mmol/L组的精子畸形率第1、4天分别低于未添加组7.00%、7.31%。0.30 mmol/L组的精子畸形率第3、5天均低于其他组,且分别比未添加组低了11.74%、4.70%。0.45 mmol/组的畸形率第3、4天分别低于未添加组5.87%、17.61%。0.60 mmol/L组的精子畸形率第1、3、4天分别低于未添加组1.81%、1.44%、5.87%,但以上各处理组与未添加组间差异不显著(P>0.05)。各处理组随着保存天数的增加,畸形数略有增加。
3.2 α-酮戊二酸对猪精液冷冻保存的影响
由表7可知,0.30 mmol/L组的精子活力高于未添加组0.10%,但差异不显著(P>0.05)。
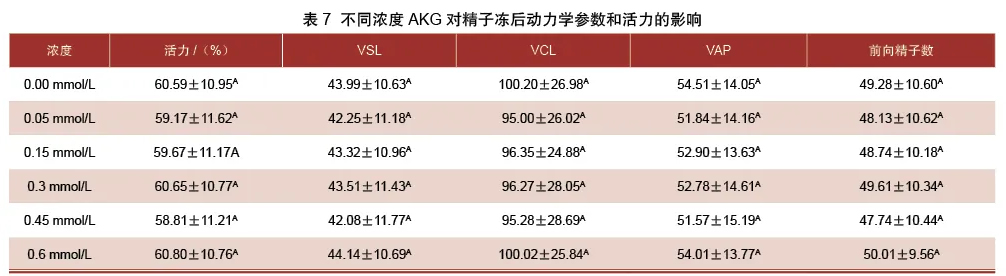
0.60 mmol/L组的精子活力、VSL分别高于未添加组0.35%、0.34%,但差异不显著(P>0.05)。与未添加组相比,0.30 mmol/L、0.60 mmol/L组的前向精子数分别高于未添加组0.67%、1.48%,但差异不显著(P>0.05)。
4
讨论与结论
4.1 AKG含量对常温保存猪精液的影响
在养猪生产中,精液常温保存技术应用较为广泛,精液可有效保存3~5 d。本研究也发现常温保存3~5 d对精子活力无显著影响,但在第6天时显著降低,这与戈新的研究一致。新鲜精液富含超氧化物歧化酶、谷胱甘肽过氧化酶、辅酶Q10等抗氧化系统相关酶,在保存初期可抵抗氧化带来的有害影响,但随着时间延长、有害物质累积、精子活性氧增多,发生氧化反应。活性氧是精子的代谢副产物,主要包括超氧阴离子、含氧自由基、过氧化物等。少量活性氧对于精子获能、发生顶体反应等生理过程是必要的。但活性氧具有较高的化学反应活性,大量堆积就有可能使精子发生氧化应激并造成精子损伤,活性氧的累积是目前精液保存面临的问题之一。因此,在精液常温保存稀释液中添加抗氧化剂,成为当前精液保存的研究热点之一。谢东淇研究发现,基础液中添加0.1 g/L壳聚糖能有效延长精液保存时间,提高保存效果,抑制细菌繁殖。宋伟报道,在稀释液中添加一定量的褪黑素,对内蒙古绒山羊精子相关运动参数具有积极的影响。在精液中添加适量的褪黑素,可以减少自由基对精子线粒体的损伤,提高精子在体外的存活时间和活力。朱林炜研究表明,在稀释液中添加1 mmol/L谷胱甘肽可显著降低猪精子丙二醛含量,提高超氧化物歧化酶活性,提高精子抗氧化性能。何兰花等研究发现,添加维生素E的猪精液常温保存稀释液能够有效提高精子活率,从而改善精液品质。
目前AKG研究主要是作为日粮添加剂提高畜禽肠道抗氧化能力。AKG可以通过与H2O2反应分解过氧化物,超氧化物歧化酶、谷胱甘肽过氧化物酶和过氧化氢酶活性来防止脂质过氧化,还可以参与机体谷胱甘肽的合成,提高谷胱甘肽的含量。黄芳等发现,在精子获能液中添加15 mmol/L AKG可以显著提高精子的获能状态,并显著提高获能过程中的糖代谢及抗氧化能力。本研究结果表明,添加不同浓度AKG,精子活力在第4~5天整体降低,其原因可能是活性氧的堆积和微生物滋生所致。过量的活性氧会对精子的结构和功能产生损伤,微生物的滋生也会消耗精子营养物质,对精子造成损伤。第5天在0.05、0.15、0.30、0.45 mmol/L组的精子活力均高于未添加组,说明添加AKG对精子活力有一定抗氧化作用,且0.30 mmol/L组的精子活力最好。而0.15 mmol/L组的1~2 d精子活力较好,但第6天显著降低,说明添加0.15 mmol/LAKG有利于短时间精液的保存。对比不同浓度AKG对精子的影响,常温保存时添加0.30 mmol/L AKG对精子抗氧化能力有一定作用。本试验结果表明,在常温保存液中添加不同浓度AKG起到了一定的抗氧化作用,对精子活力、VAP、VCL、VSL、前向精子数、畸形率无显著。
4.2 AKG含量对冷冻保存猪精液的影响
冷冻和解冻是精子冷冻保存的两个主要步骤,精液在冷冻保存过程会受到热、机械、化学和渗透压的影响,从而导致活力大幅度下降。冷冻精液解冻后的活力和运动参数是检测精子质量的重要指标。精子的活力直接影响精子的受精能力,是评定冻精解冻后精液品质和能否用于人工授精的重要指标。猪的精子膜中含有大量的多不饱和脂肪酸和胆固醇,并且胆固醇分子呈不对称分布,外单层比内层含有更多的胆固醇,因此精子膜对氧化应激和膜脂过氧化特别敏感。Klijn等研究发现,猪精液在冷冻过程中容易受温度的影响,使精子遭受氧化损伤,运动功能降低。而抗氧化剂能够抵抗氧化应激,提高冷冻保存的精子质量,因此抗氧化剂一直是精液冷冻方面的研究热点。适当添加抗氧化剂及其他保护成分有助于改善精液品质,可以有效降低所受活性氧自由基的攻击。Pei等对冷冻公猪精子质量的研究显示芹菜素和阿魏酸的联合作用显著改善了冷冻后精子的活率(P<0.05)。本研究表明,添加0.60 mmol/LAKG的精子活力、VSL、前向精子数较好,说明AKG对精子抗氧化能力有一定作用。
5
小结
AKG作为抗氧化剂,添加猪精液常温保存液或冷冻稀释液中对精子活力、运动学参数、畸形数、前向精子数均无显著影响。
|
